১১ অধ্যায় জীবাশ্ম জ্বালানি (Fossil Fuel)
জীবাশ্ম জ্বালানি (Fossil Fuel)
বহু প্রাচীনকালের উদ্ভিদ এবং প্রাণীর মৃতদেহের যে ধ্বংসাবশেষ মাটির নিচে পাওয়া যায় তাকে জীবাশ্ম বলে। বায়ুর অনুপস্থিতিতে তাপ, চাপ আর রাসায়নিক পরিবর্তনের কারণে বড় বড় উদ্ভিদ ও প্রাণী থেকে শুরু করে ক্ষুদ্রতম উদ্ভিদ ও প্রাণী পর্যন্ত সকল ধরনের উদ্ভিদ ও প্রাণী থেকে জীবাশ্ম জ্বালানির সৃষ্টি হয়েছে। কয়লা, পেট্রোলিয়াম এবং প্রাকৃতিক গ্যাসকে জীবাশ্ম জ্বালানি বলা হয়। জীবাশ্ম জ্বালানিগুলো একসাথে অথবা আলাদা আলাদা থাকতে পারে। যেমন- পেট্রোলিায়াম এবং প্রাকৃতিক গ্যাস একই সাথে পাওয়া যায়। বাংলাদেশের হরিপুর গ্যাসক্ষেত্রে প্রাকৃতিক গ্যাসের সাথে পেট্রোলিয়ামও পাওয়া গেছে।
প্রাকৃতিক গ্যাস (Natural Gas)
প্রাকৃতিক গ্যাসের প্রধান উপাদান হলো মিথেন (CH4) যার পরিমাণ 80% ।
এছাড়া প্রাকৃতিক গ্যাসে ইথেন (7%), প্রোপেন (6%), বিউটেন ও আইসোবিউটেন (4%), ও পেন্টেন (3%) থাকে। বাংলাদেশে যে প্রাকৃতিক গ্যাস পাওয়া গেছে তাতে (99.99%) মিথেন থাকে।
পেট্রোলিয়ামের উপাদানসমূহ ও পৃথকীকরণ
পেট্রোলিয়াম সাধারণত 5000 ফুট বা তার চেয়েও গভীরে শিলাস্তরের মধ্যে পাওয়া যায়।
যে পেট্রোলিয়াম খনি থেকে সরাসরি পাওয়া যায় তাকে অপরিশোধিত তেল (Crude Oil) বা পেট্রোলিয়াম বলে। এই অপরিশোধিত তেল অস্বচ্ছ ও দুর্গন্ধযুক্ত হয় । পেট্রোলিয়াম মূলত বিভিন্ন হাইড্রোকার্বনের মিশ্রণ এবং সরাসরি ব্যবহারের উপযোগী নয়।
এই অপরিশোধিত তেল আংশিক পাতন পদ্ধতিতে স্ফুটনাঙ্কের উপর ভিত্তি করে পৃথক করা হয়। আংশিক পাতন হলো এক ধরনের পাতন। এখানে বাষ্পকে ঠান্ডা করার জন্য লম্বা কলাম থাকে। পেট্রোলিয়াম বিভিন্ন হাইড্রোকার্বনের মিশ্রণ হওয়ায় এদের স্ফুটনাঙ্কও বিভিন্ন। আংশিক পাতনের সাহায্যে পৃথক করা হলে এ তেল থেকে পেট্রোল, গ্যাস, পেট্রোলিয়াম, ন্যাপথা, কেরোসিন, ডিজেল, প্যারাফিন, মোম ও পিচ প্রভৃতি অংশ পাওয়া যায়। এদের বৈশিষ্ট্য বর্ণনা করা হলো-
পেট্রোলিয়াম গ্যাস (Petroleum Gas)
এ অংশের স্ফুটনাঙ্ক থেকে পর্যন্ত। কার্বন সংখ্যা 1 থেকে 4 পর্যন্ত । অপরিশোধিত তেলে শতকরা দুই ভাগ পেট্রোলিয়াম গ্যাস থাকে। এ গ্যাসকে LPG (Liquefied Petroleum Gas) নামেও চিহ্নিত করা হয়। রান্নার কাজে এ গ্যাস ব্যবহার করা হয়।
পেট্রোল (গ্যাসোলিন) (Petrol)
স্ফুটনাঙ্ক থেকে । কার্বন সংখ্যা 5 থেকে 10 পর্যন্ত, অপরিশোধিত তেলে শতকরা 5 ভাগ পেট্রোল থাকে। যানবাহনের ইঞ্জিনে জ্বালানি হিসেবে গ্যাসোলিন ব্যবহার করা হয়।
ন্যাপথা (Naphtha)
স্ফুটনাঙ্ক থেকে পর্যন্ত। কার্বন সংখ্যা 7 থেকে 14 পর্যন্ত। পেট্রোলিয়ামে শতকরা 10 ভাগ ন্যাপথা থাকে। জ্বালানি ও পেট্রোকেমিক্যাল শিল্পে ব্যবহার করা হয়।
কেরোসিন (Kerosene)
স্ফুটনাঙ্ক থেকে পর্যন্ত। কার্বন সংখ্যা 11 থেকে 16 পর্যন্ত। পেট্রোলিয়ামে শতকরা 13 ভাগ কেরোসিন থাকে। জেট ইঞ্জিনের জ্বালানি হিসেবে ব্যবহার করা হয়।
ডিজেল (Diesel)
স্ফুটনাঙ্ক থেকে পর্যন্ত। কার্বন সংখ্যা 17 থেকে 20 পর্যন্ত। যানবাহনের জ্বালানি ও পিচ্ছিলকারক পদার্থ ও দ্রাবক হিসেবে ব্যবহার করা হয়।
প্যারাফিন মোম (Paraffin wax)
স্ফুটনাঙ্ক থেকে পর্যন্ত। কার্বন সংখ্যা 20 থেকে 30 পর্যন্ত। টয়লেট্রিজ ও ভ্যাসলিন তৈরিতে ব্যবহৃত হয়।
পিচ (Pitch)
স্ফুটনাঙ্ক উচ্চ তাপমাত্রা পর্যন্ত। কার্বন সংখ্যা 30 এর বেশি। রাস্তা তৈরিতে এটি কাজে লাগে।
হাইড্রোকার্বন (Hydrocarbon) ও অ্যালকেন (Alkane) প্রস্তুতি
কার্বন ও হাইড্রোজেনের সমন্বয়ে গঠিত যৌগকে হাইড্রোকার্বন বলে। যেমন- , , সাইক্লোহেক্সেন , । হাইড্রোকার্বন মূলত দুই প্রকার। যথা-
(i) অ্যালিফেটিক হাইড্রোকার্বন
(ii) অ্যারোমেটিক হাইড্রোকার্বন
অ্যালিফেটিক হাইড্রোকার্বন ( Aliphatic Hydrocarbons )
 |  |  |
| ইথেন | ইথিন | ইথাইন |
অ্যালিফেটিক অর্থ চর্বিজাত। অ্যালিফেটিক হাইড্রোকার্বন প্রাণীর চর্বি থেকে পাওয়া যায়।
অ্যালিফেটিক হাইড্রোকার্বন দুই ধরনের। যথা-
(i) মুক্ত শিকল হাইড্রোকার্বন
(ii) বদ্ধ শিকল হাইড্রোকার্বন
মুক্ত শিকল হাইড্রোকার্বন (Open chain Hydrocarbon)
যে সকল হাইড্রোকার্বনের কার্বন শিকলের দুই প্রান্তের কার্বন দুইটি মুক্ত অবস্থায় থাকে তাদেরকে মুক্ত শিকল হাইড্রোকার্বন বলে। যেমন-
মুক্ত শিকল হাইড্রোকার্বন আবার দুই ধরনের। যথা-
(i) সম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন
(ii) অসম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন
সম্পৃক্ত মুক্তশিকল হাইড্রোকার্বন (Saturated Open Chain Hydrocarbon)
যে মুক্ত শিকল হাইড্রোকার্বনে কার্বন কার্বন একক বন্ধন থাকে তাকে সম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন বলে। যেমন-
অসম্পৃক্ত মুক্তশিকল হাইড্রোকার্বন (Unsaturated Open Chain Hydrocarbon)
যে মুক্ত শিকল হাইড্রোকার্বনে কার্বন-কার্বন দ্বিবন্ধন বা ত্রিবন্ধন বিদ্যমান তাকে অসম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন বলে। যেমন-
বদ্ধ শিকল হাইড্রোকার্বন (Close chain Hydrocarbon)
যে সকল হাইড্রোকার্বনের কার্বন শিকলের দুই প্রান্তে কার্বন যুক্ত হয়ে একটি বলয় বা চক্র গঠন করে তাকে বদ্ধ শিকল হাইড্রোকার্বন বলে। এটিও দুই প্রকার-
(i) সম্পৃক্ত বদ্ধ শিকল হাইড্রোকার্বন । যেমন-
সাইক্লোপ্রোপেন

(ii) অসম্পৃক্ত বদ্ধ শিকল হাইড্রোকার্বন । যেমন-
সাইক্লোপ্রোপিন

বদ্ধশিকল হাইড্রোকার্বনকে অ্যালিসাইক্লিক হাইড্রোকার্বন বলে।
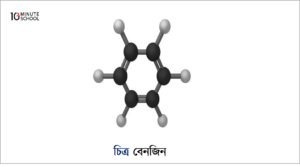
অ্যারোমেটিক হাইড্রোকার্বন (Aromatic hydrocarbons)
গ্রীক শব্দ অ্যারেমা থেকে অ্যারোমেটিক শব্দটি এসেছে যার অর্থ হলো- সুগন্ধ। যেমন-
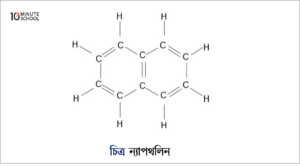
বেনজিন , ন্যাপথলিন
 |
|
| বেনজিন | ন্যাপথলিন |
সমগোত্রীয় শ্রেণি (Homologous Series)
যে সকল যৌগের কার্যকরী মূলক একই এবং তাদের ভৌত রাসায়নিক ধর্মের গভীর মিল থাকে তারা একই শ্রেণিভুক্ত । এদেরকে সমগোত্রীয় শ্রেণি বলে।
| সমগোত্রীয় শ্রেণি | সাধারণ সংকেত | প্রথম কয়েকটি সদস্যের নাম ও সংকেত |
| অ্যালকেন | মিথেন , , প্রোপেন , বিউটেন | |
| অ্যালকিন | ||
| অ্যালকাইন | ||
| অ্যালকোহল | ||
| অ্যালডিহাইড | ইথান্যাল ( , প্রোপান্যাল | |
| কার্বক্সিলিক এসিড | ইথানয়িক এসিড ( ), প্রোপানয়িক এসিড |
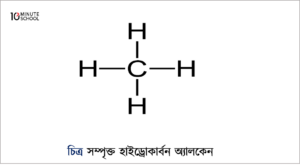
সম্পৃক্ত হাইড্রোকার্বন অ্যালকেন ( Saturated Hydrocarbons : Alkanes)
যে সকল হাইড্রোকার্বনে কার্বন কার্বন একক বন্ধন বিদ্যমান তাকে অ্যালকেন বলে। এর প্রথম সদস্যের নাম মিথেন (CH4), এর বন্ধন ভাঙ্গা অনেক কঠিন। তাই অ্যালকেন রাসায়নিক ভাবে নিষ্ক্রিয়। তাই এদেরকে প্যারাফিন বলা হয়। (প্যারাফিন অর্থ আসক্তিহীন )
অ্যালকেনের নামকরণ (Naming Alkanes)
IUPAC পদ্ধতিতে-
(i) সরল শিকল বিশিষ্ট অ্যালকেনে এক কার্বনবিশিষ্ট অ্যালকেনকে মিথেন, দুই কার্বনবিশিষ্ট অ্যালকেনকে ইথেন বলে।
(ii) কার্বন সংখ্যার গ্রিক-সংখ্যাসূচক শব্দের শেষে এন(ane) যোগ করে নামকরণ করা হয়।
অ্যালকাইল মূলক ( Alkyl Group )
অ্যালকেন থেকে একটি H পরমাণু অপসারণ করলে যে একযোজী মূলকের সৃষ্টি হয় তাকে অ্যালকাইল মূলক বলে। এর সাধারণ সংকেত যেমন- – (মিথাইল), (ইথাইল)
অ্যালকেনের প্রস্তুতি (Alkanes preparation)
কার্বন ডাই অক্সাইড থেকে অ্যালকেন (Alkane from carbon dioxide)
নিকেল প্রভাবকের উপস্থিতিতে কার্বন ডাই অক্সাইডের সাথে কে তাপমাত্রায় এ উত্তপ্ত করলে মিথেন ও পানি উৎপন্ন হয়।
অ্যালকিন ও অ্যালকাইন থেকে অ্যালকেন (Alkane from alkyne and alkyne)
Ni প্রভাবকের উপস্থিতিতে পৃথকভাবে ইথিন ও ইথাইনের সাথে কে তাপমাত্রায় উত্তপ্ত করলে ইথেন উৎপন্ন হয়।
ডিকার্বক্সিলেশন বিক্রিয়ার মাধ্যমে অ্যালকেন প্রস্তুতি (Alkane production through decarboxylation reaction)
এর উপস্থিতিতে সোডিয়াম ইথানয়েটকে সোডিয়াম হাইড্রোক্সাইডের সাথে উত্তপ্ত করলে মিথেন ও সোডিয়াম কার্বনেট উৎপন্ন হয়। এই বিক্রিয়াকে ডিকার্বক্সিলেশন বিক্রিয়া বলে।
অ্যালকেনের ধর্ম (Alken’s characteristics)
অ্যালকেনের ভৌত ধর্ম (Physical property)
সম্পৃক্ত অ্যালকেনের কার্বন সংখ্যার পরিবর্তন হলে ভৌত অবস্থার পরিবর্তন হয়।
- 1 থেকে 4 কার্বন সংখ্যার সম্পৃক্ত অ্যালকেনের স্ফুটনাঙ্ক কক্ষ তাপমাত্রার নিচে, তাই এগুলো গ্যাসীয় অবস্থায় থাকে।
- 5 থেকে 15 কার্বন সংখ্যা হলে এগুলো তরল স্ফুটনাঙ্ক 36.1°C ।
- কার্বন সংখ্যা 16 এর বেশি হলে কঠিন প্রকৃতির হয়।
অ্যালকেনের রাসায়নিক ধর্ম (Chemical Property)
অ্যালকেনসমূহ রাসায়নিকভাবে নিষ্ক্রিয়। তবুও এরা কিছু রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে। যেমন-
ক্লোরিনের সাথে অ্যালকেনের বিক্রিয়া
অতিবেগুনি আলোর উপস্থিতিতে মিথেনের সাথে ক্লোরিন মিশ্রিত করলে টেট্রাক্লোরো মিথেন উৎপন্ন হয়। এই বিক্রিয়া চার ধাপে সম্পন্ন হয়।
এই চার ধাপে উৎপন্ন উৎপাদগুলো বিভিন্ন কাজে ব্যবহার হয়ে থাকে।
মিথেন মৃদু সূর্যালোকের উপস্থিতিতে বিক্রিয়া করে। মিথাইল ক্লোরাইড , ডাইক্লোরোমিথেন , ট্রাইক্লোরো মিথেন , টেট্রাক্লোরোমিথেন এর মিশ্রণ উৎপন্ন করে।
- মিথাইল ক্লোরাইড শিল্পক্ষেত্রে অ্যালকোহল, অ্যালডিহাইড, জৈব এসিড প্রস্তুতিতে ব্যবহৃত হয়।
- ডাইক্লোরোমিথেন ইমালশন, রং শিল্পে দ্রাবক হিসেবে ব্যবহার করা হয়।
- ক্লোরোফরম কে চেতনানাশক হিসেবে এবং
- কার্বন টেট্রাক্লোরাইড কে ড্রাইওয়াশে দ্রাবক হিসেবে ও অগ্নিনির্বাপক হিসেবে ব্যবহার করা হয়।
এর সাথে দহন বিক্রিয়া
বায়ুর এর সাথে বিক্রিয়া করে , জলীয় বাষ্প ও তাপশক্তি উৎপন্ন করে।
অ্যালকাইন, অ্যালকোহল, অ্যালডিহাইড ও জৈব এসিড
অ্যালকাইন ( Alkynes)
যে জৈব যৌগে কার্বন শিকলে অন্তত একটি কার্বন কার্বন ত্রিবন্ধন (-C≡C-) থাকে তাকে অ্যালকাইন বলে। অ্যালকাইনের সাধারণ সংকেত । এর প্রথম সদস্য হলো ইথাইন বা এসিটিলিন।
অ্যালকাইনের নামকরণ
অ্যালকেনের নামের শেষে এন বাদ দিয়ে আইন উচ্চারণ করা হয়। যেমন- (ইথাইন)
অ্যালকাইনের প্রস্তুতি
- ক্যালসিয়াম কার্বাইড থেকে
ক্যালসিয়াম কার্বাইডের মধ্যে পানি যোগ করলে ইথাইন এবং উৎপন্ন হয়।
অ্যালকাইনের রাসায়নিক ধর্ম
- হাইড্রোজেন সংযোজন
প্রভাবকের উপস্থিতি ইথাইনকে এর সাথে তাপমাত্রায় উত্তপ্ত করলে ইথেন উৎপন্ন হয়।
- পানি সংযোজন
তাপমাত্রায় ইথাইনের মধ্যে 20% সালফিউরিক এসিড এবং 2% মারকিউরিক সালফেট দ্রবণ যোগ করলে ইথান্যাল উৎপন্ন হয়।
অ্যালকোহল (Alcohol)
যে জৈব যৌগে হাইড্রক্সিল মূলক (-OH) বিদ্যমান থাকে সে সকল যৌগকে অ্যালকোহল বলে। অ্যালকোহলের সাধারণ সংকেত । এর প্রথম সদস্য মিথানল । অ্যালকোহলকে R-OH দিয়ে প্রকাশ করা যায়, যেখানে R হলো অ্যালকাইল মূলক। এ শ্রেণীর ১ম দিকের সদস্যগুলো বর্ণহীন তরল পদার্থ এবং পানিতে সকল অনুপাতে মিশ্রিত হয়।
অ্যালকোহলের নামকরণ
অ্যলেকেনের নামের শেষের (e) বাদ দিয়ে অল (Ol) যোগ করে অ্যালকোহলের নামকরণ করা হয়। যেমন-
ইথানল
অ্যালকোহল প্রস্তুতি
ইথাইল ব্রোমাইড থেকে
ব্রোমো ইথেনের মধ্যে সোডিয়াম হাইড্রোক্সাইডের জলীয় দ্রবণ যোগ করলে ইথানল এবং সোডিয়াম ব্রোমাইড উৎপন্ন হয়।
অ্যালডিহাইড ( Aldehyde)
যে জৈব যৌগে অ্যালডিহাইড গ্রুপ বিদ্যমান থাকে তাকে অ্যালডিহাইড বলে।
অ্যালডিহাইডের নামকরণ (Naming of aldehydes)
অ্যালকেনের নামের শেষে (এন) বাদ দিয়ে (অ্যাল) যোগ করে অ্যালডিহাইডের নামকরণ করা হয়। যেমন-
(প্রোপান্যাল)
অ্যালডিহাইডের প্রস্তুতি (Preparation of aldehydes)
- পানি সংযোজন
তাপমাত্রায় ইথাইনের মধ্যে এসিড এবং 2% মারকিউরিক সালফেট দ্রবণ যোগ করলে ইথান্যাল উৎপন্ন হয়।
ফরমালিন (Formalin)
ফরমালডিহাইড (মিথান্যাল) এর 40% জলীয় দ্রবণকে ফরমালিন বলে। ফরমালিনে 40 ভাগ মিথান্যাল আর 60 ভাগ পানি থাকে। মৃত প্রাণীর দেহ সংরক্ষণ করার জন্য ফরমালিন ব্যবহার করা হয়।
জৈব এসিড বা ফ্যাটি এসিড (Fatty Acid)
যে জৈব যৌগে কার্বক্সিল গ্রুপ (-COOH) বিদ্যমান থাকে তাকে জৈব এসিড বা ফ্যাটি এসিড বলে। জৈব এসিডের সাধারণ সংকেত । সংক্ষেপে একে R-COOH দিয়ে প্রকাশ করা হয়।
জৈব এসিডের নামকরণ (Naming of organic acids)
অ্যালকেনের নামের শেষে এন বাদ দিয়ে অয়িক এসিড যুক্ত করে জৈব এসিডের নামকরণ করা হয়। যেমন-
ইথানয়িক এসিড
জৈব এসিডের প্রস্তুতি (Preparations of fatty acids)
ইথান্যাল থেকে
ইথান্যালের মধ্যে লঘু এসিড এবং পটাশিয়াম ডাইক্রোমেট যোগ করলে জারণ বিক্রিয়ার মাধ্যমে ইথানয়িক এসিড উৎপন্ন হয়।
ফ্যাটি এসিডের রাসায়নিক ধর্ম (The chemical nature of fatty acids)
অম্লীয় ধর্ম
সকল ফ্যাটি এসিড হলো দুর্বল এসিড। ফ্যাটি এসিডসমূহ জলীয় দ্রবণে সামান্য পরিমাণে বিয়োজিত হয়। এর জলীয় দ্রবণ নীল লিটমাসকে লাল করে। ক্ষারের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে। যেমন-
ভিনেগার
ইথানয়িক এসিডের 6-10% জলীয় দ্রবণকে ভিনেগার বলে। ভিনেগার খাবার তৈরিতে ও খাদ্য সংরক্ষক হিসেবে কাজ করে।
অ্যালকেন থেকে অ্যালকোহল, অ্যালডিহাইড ও জৈব এসিড তৈরি (Alcohol, Aldehyde, and Organic Acid Preparation from Alkane)
ধাপ -১
ধাপ -২
ধাপ -৩
[ এর বিক্রিয়ার ফলে [O] তৈরি হয়। ]
ধাপ -৪
যদি যে কোনো অ্যালকেন থেকে অ্যালকোহল, অ্যালডিহাইড থেকে জৈব এসিড তৈরি করতে বলা হয়, তাহলে উপরের ধাপগুলো মাথায় রেখে করলেই হবে।
অ্যালকিন থেকে অ্যালকোহল, অ্যালডিহাইড এবং কার্বক্সিলিক এসিড তৈরি (Alcohol, Aldehyde and Carboxylic Acid Preparation from Alkene)
ধাপ – ১
ধাপ – ২
ধাপ – ৩
ধাপ – ৪
অ্যালকেন আর অ্যালকিনের থেকে প্রস্তুতির ধাপগুলো একই, শুধুমাত্র্র প্রথম ধাপটি আলাদা।
আরো কয়েকটি গুরুত্বপূর্ণ রুপান্তর
ইথেন থেকে ইথিন (Ethane to Ethene)
ধাপ -১
ধাপ -২
মিথেন থেকে ইথিন (Methane to Ethene)
মিথেন থেকে ইথাইন (Methane to Ethyne)
ব্যবহার (Usage)
অ্যালকোহলের ব্যবহার (Use of Alcohol)
(১) মিথানল বিষাক্ত রাসায়নিক পদার্থ। মিথানল মূলত অন্য রাসায়নিক পদার্থ প্রস্তুত করতে ব্যবহৃত হয়।
(২) রাসায়নিক শিল্পে ইথানয়িক এসিড বিভিন্ন জৈব এসিডের এস্টার প্রস্তুত করা হয়।
(৩) ইথানলকে প্রধানত পারফিউম, কসমেটিকস ও ঔষধ শিল্পে দ্রাবক হিসেবে ব্যবহার করা হয়।
(৪) ইথানলের 96% জলীয় দ্রবণকে রেকটিফাইড স্পিরিট বলে।
(৫) ঔষধ ও খাদ্য শিল্প ব্যতিত অন্য শিল্পে রেকটিফাইড স্পিরিট সামান্য মিথানল যোগে বিষাক্ত করে ব্যবহার করা হয়।
(৬) জীবাশ্ম জ্বালানির পরিবর্তে ইথানলকে মোটর ইঞ্জিনের জ্বালানিরূপে ব্যবহার করা হচ্ছে।
অ্যালডিহাইডের ব্যবহার (Use of Aldehyde)
অ্যালডিহাইডের পলিমারকরণ বিক্রিয়ায় বিভিন্ন প্লাস্টিক দ্রব্য তৈরি করা হয়।
(১) মিথান্যালের জলীয় দ্রবণকে অতি নিম্ন বাষ্পে উত্তপ্ত করলে ডেরালিন পলিমার উৎপন্ন হয়। ডেরালিন পলিমার দিয়ে চেয়ার, টেবিল, বালতি ইত্যাদি প্লাস্টিক দ্রব্য তৈরি করা হয়।
(২) ফরমালডিহাইড ও ইউরিয়া ফরমালডিহাইড রেজিন উৎপন্ন হয় যা গৃহের প্লেট, গ্লাস, মগ তৈরিতে ব্যবহৃত হয়।
জৈব এসিডের ব্যবহার (Use of Organic acid)
(১) জৈব এসিড মানুষের খাদ্যোপযোগী উপাদান। আমরা লেবুর রস, তেঁতুল, দধি ইত্যাদিতে উপস্থিত জৈব এসিডকে খাবার হিসেবে গ্রহণ করি।
(২) জৈব এসিডের ব্যাকটেরিয়া ধ্বংস করার ক্ষমতা রয়েছে।
(৩) ইথানয়িক এসিডের 6% থেকে 10% জলীয় দ্রবণকে ভিনেগার বলা হয়। ভিনেগার সস ও আচার সংরক্ষণে ব্যবহৃত হয়।
পলিমার (Polymar) প্রকারভেদ, ধর্ম ও ব্যবহার
পলিমার ( Polymar )
যে বিক্রিয়ায় কোনো পদার্থের অনেকগুলো ক্ষুদ্র অণু পরস্পর যুক্ত হয়ে বৃহৎ অণু গঠন করে সেই বিক্রিয়াকে পলিমারকরণ বিক্রিয়া বলে। এর একটি অণুকে মনোমার বলা হয়। একাধিক মনোমার মিলে পলিমার গঠিত হয়। আমাদের খাদ্যের প্রধান উপাদান প্রোটিন হলো অ্যামাইনো এসিডের একটি পলিমার (Polymar)।
বি: দ্র: মনো এর অর্থ “একটি”, পলি এর অর্থ “বহু”।
পলিমারকরণ বিক্রিয়া দুই প্রকার। যথা-
(i) সংযোজন বা যুত পলিমার
(ii) ঘনীভবন পলিমার
সংযোজন বা যুত পলিমার (Addition or additive polymer)
যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুগুলো সরাসরি একে অপরের সাথে যুক্ত হয়ে দীর্ঘ শিকল বিশিষ্ট পলিমার গঠন করে তাকে সংযোজন পলিমারকরণ বিক্রিয়া বলে।
সংযোজন পলিমারকরণ বিক্রিয়া
সামান্য পরিমাণ অক্সিজেনের উপস্থিতিতে 1000 বায়ুমন্ডল চাপে (atm) ও তাপমাত্রায় ইথিনকে উত্তপ্ত করলে পলিথিন উৎপন্ন হয়। এই বিক্রিয়ায় ইথিনকে মনোমার বলা হয়।
পলিপ্রোপিন
প্রোপিনকে টাইটানিয়াম ক্লোরাইডের উপস্থিতিতে চাপে তাপমাত্রায় উত্তপ্ত করলে পলিপ্রোপিন উৎপন্ন হয়।
পলিপ্রোপিন দিয়ে দড়ি, পাইপ, কার্পেট প্রভৃতি তৈরি করায় এটি পলিথিনের চেয়ে শক্ত এবং হালকা ।


পলিভিনাইল ক্লোরাইড (PVC)
ভিনাইল ক্লোরাইডকে জৈব পার অক্সাইডের উপস্থিতিতে উচ্চ চাপ ও তাপমাত্রায় উত্তপ্ত করলে পলিভিনাইল ক্লোরাইড (PVC) উৎপন্ন হয়।
ঘনীভবন পলিমার ( Condensation Polymer)
যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুসমূহ পরস্পরের সাথে যুক্ত হবার সময় ক্ষুদ্র ক্ষুদ্র অণু, যেমন- ইত্যাদি অপসারণ করে সেই পলিমারকরণকে ঘনীভবন পলিমারকরণ বিক্রিয়া বলে।
নাইলন 6:6 উৎপাদন
টাইটানিয়াম অক্সাইডের উপস্থিতিতে হেক্সামিথিলিন ডাই অ্যামিন এর সাথে অ্যাডিপিক এসিড উত্তপ্ত করলে নাইলন -6:6 উৎপন্ন হয়।

উৎসের উপর ভিত্তি করে পলিমারকে আবার দুই ভাগে করা যায়। যথা-
- প্রাকৃতিক পলিমার
- কৃত্রিম পলিমার
প্রাকৃতিক পলিমার
প্রাকৃতিকভাবে অনেক পলিমার উৎপন্ন হয়। যেমন- উদ্ভিদের সেলুলোজ ও স্টার্চ দু’টোই প্রাকৃতিক পলিমার। যা বহুসংখ্যক গ্লুকোজ অণু থেকে তৈরি হয়। রাবার গাছের কষ একটি প্রাকৃতিক পলিমার।
কৃত্রিম পলিমার বা প্লাস্টিক
শক্ত, হালকা, সস্তা এবং যেকোনো পছন্দসই রঙের প্লাস্টিক পাওয়া যায়। প্লাস্টিককে গলানো যায় এবং ছাঁচে ঢেলে যেকোনো আকার দেওয়া যায়। প্লাস্টিক শব্দটি গ্রীক ভাষা থেকে এসেছে। যার অর্থ গলানো সম্ভব। বর্তমানে প্লাস্টিকের ব্যবহার ব্যাপক।
বিভিন্ন ধরনের পলিমার, তার ধর্ম ও ব্যবহার (Different types of polymers, their properties and uses)
| পলিমারের নাম | মনোমারের সংকেত | পলিমারের ধর্ম | ব্যবহার |
| পলিথিন | টেকসই | প্লাস্টিক ব্যাগ, প্লাস্টিক শিট | |
| পলিপ্রোপিন | টেকসই | প্লাস্টিক রশি, কার্পেট, প্লাস্টিক বোতল | |
| পলিভিনাইল ক্লোরাইড (PVC) | শক্ত, কঠিন এবং পলিথিনের তুলনায় কম নমনীয় | পানির পাইপ, বিদুৎ অপরিবাহী পদার্থ | |
| নাইলন 6:6 | ও | চকচকে, টেকসই, নমনীয় | কৃত্রিম কাপড়, রশি, দাঁতের ব্রাশ |
জৈব ও অজৈব যৌগের পার্থক্য:
| জৈব যৌগ | অজৈব যৌগ |
| (i) কার্বন অবশ্যই থাকবে | (i) ব্যতিক্রমগুলো ছাড়া কার্বন থাকে না । যেমন− |
| (ii) বিক্রিয়া সম্পন্ন হতে অনেক সময় লাগে। | (ii) বিক্রিয়া হতে কম সময় লাগে। |
| (iii) সমযোজী বন্ধনের মাধ্যমে গঠিত হয়। | (iii) আয়নিক বা সমযোজী বন্ধনের মধ্যমে গঠিত হয়। |

Comments
Post a Comment
Thanks